| CLASIF. DE LA MATERIA. SUSTANCIAS PURAS Y MEZCLAS |
|---|
| CLASIFICACIÓN DE LA MATERIA |
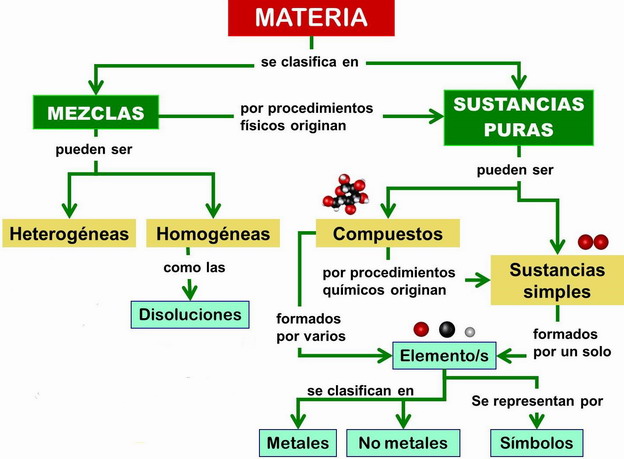 |
| Materia o mezcla heterogénea | Aquélla que a simple vista o con el microscopio óptico se distinguen partes distintas. Distintas porciones de la misma presentan apariencias diferentes. Están constituidas por dos o más clases de moléculas o componentes (en cualquier proporción). Sus prop. son variables porque dependen de la proporción de los comp. mezclados, y se pueden desdoblar en sus comp. por procedimientos físicos. |
|
| Suspensiones → las part. de un sólido están dispersas en un líquido. | ||
| Emulsiones → formadas por líquidos inmiscibles (de densidades distintas) agitados. | ||
| Materia o mezcla homogénea | Aquélla que a simple vista o con el microscopio óptico no se distinguen partes distintas. Distintas porciones de la misma presentan la misma apariencia. | |
| Sust. pura | Mat. homogénea de composición cte. Están constituidas por un solo componente y tienen una sola clase de moléculas. No se pueden desdoblar en otras sust. por procedimientos físicos. Cada sust. pura tiene unas prop. características ctes., que las distingue unas de otras: - Puntos de fusión y de ebullición - Calor específico - Densidad,... |
|
| Simples o elementos químicos Sust. puras que no pueden descomponerse en otras más sencillas. Son moléculas formadas por una sola clase de átomos. Cada elem. se representa por una abreviatura → símbolo químico. |
||
| Compuestos o combinaciones químicas Sust. puras que pueden descomponerse en otras más sencillas mediante métodos químicos. Son moléculas formadas por más de una clase de átomos. Cada combinación química se representa mediante una expresión abreviada → fórmula química, formada por los símbolos de los elem. químicos que constituyen su molécula. |
||
| Disoluciones | Mat. homogénea de composición variable . Están constituidas por dos o más clases de moléculas o componentes (en cualquier proporción). Sus prop. son variables porque dependen de la proporción de los comp. mezclados, y se pueden desdoblar en sus comp. por procedimientos físicos. |
|
| Soluto → el que se disuelve; se encuentra en menor cantidad. Disolvente → sust. que disuelve al soluto; se encuentra en mayor cantidad. |
||
Las sust. puras pueden ser homogéneas (agua) o heterogéneas (agua + hielo). Lo mismo para las mezclas (homogéneas: agua + sal; heterogéneas: agua + arena).
Comprobar que en la mezcla agua + alcohol, no se conserva el volumen (aunque sí la masa).
| PROCESOS FÍSICOS Y QUÍMICOS |
- Cambio o proceso físico → es aquel que no altera las sust. que intervienen; es reversible.
- Cambio o proceso químico → es aquel que altera las sust. que intervienen, transformándolas en otras sust. dif.; en gen., es irreversible.
Ej.:
La electrólisis descompone el H2O en H2 y O2.
El CaCO3 sufre una descomposición térmica en CO2 + CaO (cal viva).
Las mezclas son cambios físicos. Las combinaciones son cambios químicos.
| DIFERENCIAS ENTRE MEZCLA Y COMBINACIÓN QUÍMICA |
|
MEZCLA
|
COMBINACIÓN QUÍMICA
|
| Las sust. integrantes conservan sus propiedades. El proceso, en gen., es reversible. |
Las prop. de la combinación resultante son dif. a las de las sust. integrantes. El proceso, en gen., es irreversible. |
| Las sust. integrantes pueden agruparse en cualquier proporción. | Las sust. integrantes deben intervenir en proporciones fijas y determinadas. |
| La separación de las sust. integrantes puede realizarse mediante procedimientos físicos. | La separación de las sust. integrantes no puede realizarse por procedimientos físicos, sino sólo por procesos químicos. |
| En gen., en el proceso no existe variación de E. | En gen., en el proceso sí existe variación de E. |
Química → ciencia que estudia la estructura, el comportamiento y las prop. de la mat. de que están constituidos los cuerpos, así como tb. los fenómenos en los que dicha mat. cambia de naturaleza.
| MÉTODOS DE SEPARACIÓN DE MEZCLAS HETEROGÉNEAS |
|
MÉTODO
|
DISPOSITIVO
|
SUSTANCIAS A SEPARAR
|
EJEMPLOS
|
| Tamizado o cribado | Tamiz o criba | Dos sólidos de distinto tamaño de grano. | Lentejas y garbanzos |
| Decantación | Embudo de decantación | Dos líquidos no miscibles de distinta densidad. | Vinagre y aceite |
| Filtración | Filtro | Un sólido no disuelto en un líquido. | Agua y arena |
| Centrifugación | Centrifugadora | Sólidos no disueltos en líquidosque no se pueden separar mediante filtros. | Sangre |
| Extracción = disolución selectiva (disolución + filtración) |
Vaso de precipitados y embudo con filtro | Mezclas de dos sólidos donde uno de ellos se disuelve en un líquido y el otro no. | S y NaCl |
| Separación magnética | Vidrio de reloj + Imán con papel | Una sust. mezclada con prop. magnéticas. | Vifrutas de Fe y Al |
| Todos utilizan procesos físicos, ya que sus componentes no pierden sus prop. físicas. |
| |
| MÉTODOS DE SEPARACIÓN DE MEZCLAS HOMOGÉNEAS |
|
MÉTODO
|
DISPOSITIVO
|
SUSTANCIAS A SEPARAR
|
EJEMPLOS
|
| Cristalización Lenta → evaporación (cristales grandes) Brusca → ebullición (cristales pequeños) Por enfriamiento → magmas. |
Cristalizador | Sólidos disueltos en un líquido. | Agua + sal Aplicación: las salinas |
| Destilación (ebullición + licuación) |
Destilador | Líquidos disueltos. Se basa en la dif. de T de ebullición de cada comp. Hay que purificar. | Alcohol y agua del vino. Benceno y tolueno. |
 |
| Destilador |
| Ver MEZCLAS HOMOGÉNEAS: DISOLUCIONES. |